SP1 - GUIDE-IBD
Zentrale Koordination der klinischen Beobachtungsstudie
Im Zentrum des Verbundprojektes steht das Teilprojekt SP1, welches die klinische Beobachtungsstudie organisiert. Ziel ist es herauszufinden, ob das zusätzliche molekulares Wissen (durch die Bereitstellung neuartiger molekularer Marker) die ärztlichen Entscheidungen zur Therapie von CED-Patienten mit anti-TNF-Biologika verbessert (Medikamentenverbrauch, Krankheitskontrolle). Diese Aufgabe wird von drei Partnern aus Kiel (SP1a), Hamburg (SP1b) und Hannover (SP1c) erfüllt, wobei Kiel als führender Partner agiert.
Insgesamt werden 130 Patientinnen und Patienten mit CED, wie Morbus Crohn oder Colitis Ulcerosa, rekrutiert, die erstmalig eine Gabe von anti-TNF-Therapie (Infliximab oder ein ähnliches Medikament (Biosimilars)) erhalten. Die Indikation wird dabei durch eine lokale Therapiekonferenz gestellt und stellt somit keine Gabe von Arzneimitteln unter Studienbedingungen dar. Erst nach der Therapieentscheidung werden die Patienten gebeten, an der Studie teilzunehmen. Die Patienten werden dann mithilfe eines definierten Stratifikations- und Randomisationsalgorithmus einem Arm der Studie zugeordnet. 65 Patienten werden sich im „molecular medicine"-Arm befinden, in dem selektierte, in Vorstudien validierte Markerpanel auf verschiedenen Datenebenen (Genexpression, mikrobielle Marker, Serummarker, innovative Pharmakokinetik) bestimmt werden und dem behandelnden Arzt als Zusatzinformation vorgelegt werden. Diese zusätzlichen Daten kann der Arzt für seine weiteren Therapieentscheidungen verwenden. Die anderen 65 Patienten erhalten die Standardtherapie („best standard care"), die nach aktuellen Empfehlungen, aber ohne molekulares Zusatzwissen gesteuert wird. Auch bei diesen Patienten erfolgt die Entnahme der Biomaterialien, die durch andere Teilprojekte (SP2 und SP4) detailliert untersucht werden, aber ohne dass Ergebnisse zurück kommuniziert werden. Das Teilprojekt SP3 nutzt die Patientenbeobachtung um neue Endpunkte für Studien zu finden (kontinuierlich Erfassung von Lebensqualitätsprofilen und physischer Aktivität über tragbare Biosensoren inkl. APP). Die Entnahmematerialien werden zentral durch den führenden Partner Kiel (SP1a) bereitgestellt. Die Organisation der Proben sowie die Erhebung und Kontrolle der Patientendaten erfolgt in Kiel (SP1a), Hamburg (SP1b) und Hannover (SP1c) durch Technische/Medizinische Assistenz.
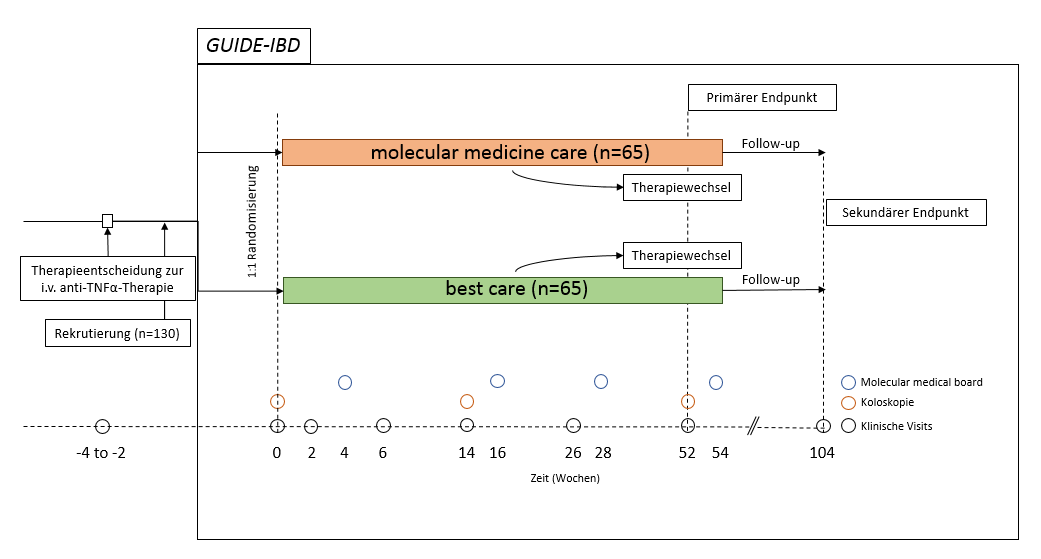
Schema der Patientenrekrutierung und Biomaterialen-Entnahme für das Molekulare Reporting. An Woche 4, 16, 28 und 54 nach Induktion werden im „Molecular Medicine Board“ die zuvor erhobenen molekularen Befunde in die weitere Therapieentscheidung miteinbezogen.



