Melanoma sensitivity
Prädiktion der individuellen Sensitivität maligner Melanomzellen gegenüber Kombinationtherapien durch statistische und Netzwerkmodellierung innovativer 3D organotypischer Testmodelle
Das maligne Melanom (MM) ist eine aggressive Entartung der Pigmentzellen (Melanozyten) der Haut, dessen Auftreten stetig zunimmt und für das metastatische Stadium eine sehr schwache Prognose bietet. Da das MM weitgehend resistent gegenüber herkömmlichen Chemo-, und Radiotherapien ist, rücken spezifische Inhibitoren aktivierter Mutanten der zellulären Signalübertragung in den Fokus. Auch diese zeigen bislang nur teilweise therapeutischen Erfolg und gehen mit einer starken Rückfallrate einher. Daher ist eine verlässliche Diganose einzelner Melanomzellen gefordert, um systematisch deren Ansprechen und Resistenzpotential analysieren und Vorhersagen treffen zu können.
Voraussetzung dafür ist das Verständnis der molekularbiologischen Prozesse innerhalb des Tumors, sowie zwischen Tumor- und Wirtsgewebe.

Prof. Dagmar Kulms hat ein 3D-Vollhautmodell entwickelt, in welches Melanom-Sphäroide definierter Anzahl und Größe eingebracht werden, die in Aufbau und Physiologie Melanom-Metastasen gleichen (WP1). Ziel ist es das Ansprechen spezifischer Inhibitoren durch zusätzliche Einleitung des programmierten Zelltodes (Apoptose) zu verbessern. Hier spielt der Todesligand TRAIL (Tumor necrosis factor related apoptosis-inducing ligand) eine Schlüsselrolle. Basierend auf TRAIL-Fc-Fusionsproteinen haben Dr. Pfizenmaier und Dr. Kontermann TRAIL-Rezeptor-Agonisten (IZI1551) entwickelt, die eine gesteigerte therapeutische Wirksamkeit aufweisen (WP4).Die Kombination aus mutationsspezifischen Therapieansätzen mit systembiologischer Modellierung bildet eine exzellente Basis für die Entwicklung prädiktiver Verfahren. Dr. Markus Rehm hat ein mathematisches Modell (SYSACT) entwickelt, das mit hoher Genauigkeit die Ansprechrate von Melanomzellen gegenüber Chemotherapeutika und TRAIL vorhersagen kann. Es basiert auf Kenntnis der apoptotischen Signalübertragung und kann die Kernentscheidung des Prozesses abbilden (WP1/2/3). Dr. Thomas Sauter hat ein großskaliges Boolesches Modell der apoptotischen Signaltransduktion entwickelt, das das Systemverhalten abbildet und eine umfassende Netzwerkbeschreibung bietet (WP2). Dr. Friedegund Meier stellt das Bindeglied zur Klinik dar, und gewährleistet die Analyse primärer Patientendaten und –proben aus einer 400 Patienten umfassenden Datenbank (WP3).
Wir möchten ein standardisiertes systembasiertes Modell entwickeln, welches die individualisierte maßgeschneiderte Melanom-Therapie vorhersagen und damit das Therapie-Ergebnis maßgeblich verbessern kann.
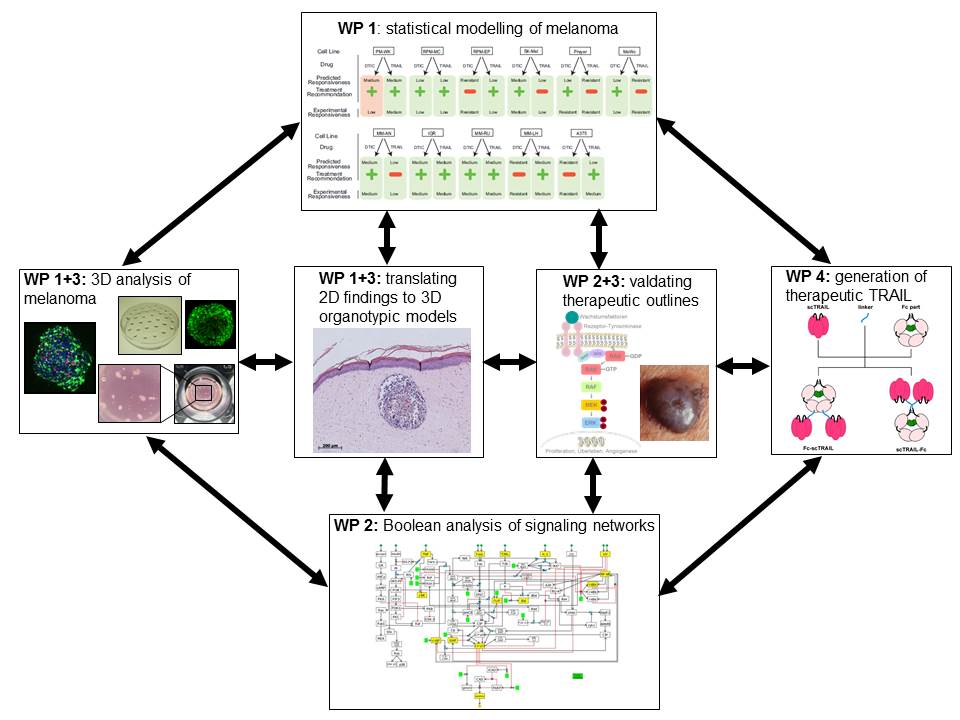
Teilprojekte in Melanoma sensitivity:
TP 2 Translation und klinische Validierung prädiktiver Marker für Therapieansprechen (SYSACT)
TP 3 Herstellung und Validierung von therapeutisch relevanten neuartigen TRAIL- Fusionsproteinen
TP 4 Herstellung und Validierung von therapeutisch relevanten neuartigen TRAIL- Fusionsproteinen



