SYS-GLIO
Systembasierte Vorhersagen für das biologische und klinische Verhalten von Gliomen
Diffus infiltrierende astrozytische Gliome sind die häufigsten intrinsischen Hirntumoren und decken ein breites Spektrum von malignen Graden ab, die von dem diffusen Astrozytom (WHO-Grad II) über das anaplastisches Astrozytom (WHO-Grad III) bis hin zu Glioblastomen (WHO Grad IV) reichen. Klinisch unterscheiden sich zwei Arten von Glioblastomen: primäre Glioblastome, die de novo entstehen und einen rapiden klinischen Verlauf haben, und sekundäre Glioblastome, die sich offenbar durch die Progression eines bereits vorhandenen niedriggradigen Glioms entwickeln. Trotz ähnlicher histologischer Eigenschaften unterscheiden sich primäre und rezidivierende Glioblastome durch distinkte genomische, epigenetische und transkriptomische Veränderungen. Glioblastome haben immer noch eine generell schlechte Prognose bei Kindern wie auch bei Erwachsenen, mit einer mittleren Überlebenszeit von weniger als 12 Monaten ab dem Zeitpunkt der Diagnose. In diesem Projekt wollen wir die genetischen Eigenschaften maligner Hirntumoren unterschiedlicher WHO Grade genauer analysieren. Mit den Ergebnissen dieser Untersuchungen wollen wir neue Strategien entwickeln, um die maligne Progression von niedriggradigen Gliomen zu stoppen und Therapieresistenzen in hochgradigen Läsionen zu verhindern.
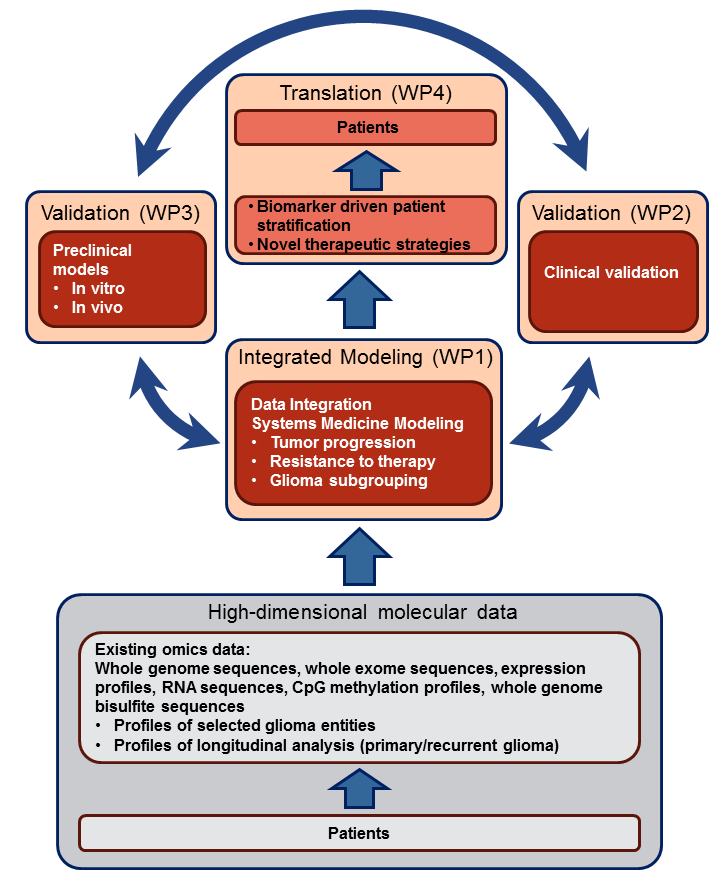
Teilprojekte in SYS-GLIO:
TP 1A Integrative Analyse genomweiter Datensätze
TP 1B Mathematische Modellierung des Gliomwachstums
TP 2A Bewertung von wichtigen Signalwegen in der Validierungskohorte
TP 2B Bewertung von wichtigen Signalwegen in der Validierungskohorte
TP 3A In vivo-Validierung molekularer Targets in Gliomen mittels Mausmodellen
TP 3B Experimentelle Modellierung von Therapieresistenz und maligner Progression von Gliomen



