TP 5
PWAS for identification of functional SNPs and key molecules in arterial injury
Erbliche kardiovaskuläre Risikofaktoren beruhen zumeist auf genetischen Varianten, die durch den Austausch einer einzelnen Base (Single Nucleotide Polymorphism = SNP) definiert sind, welche sich zu einem gewissen Prozentsatz in der Bevölkerung wiederfinden lassen. Die meisten SNPs liegen dabei nicht in proteinkodierenden Regionen des Genoms, sondern in Bereichen in denen sich genregulatorische Einheiten befinden. Diese regulatorischen Einheiten werden von speziellen Transkriptionsfaktoren erkannt, welche wiederum Einfluss auf die Transkriptionsmaschinerie nehmen und somit die Expressionsstärke der Gene regulieren. Da die genaue Basenabfolge die Rekrutierung von Transkriptionsfaktoren beeinflusst, können SNPs die Bindung von Transkriptionsfaktoren verhindern oder neue Bindungsstellen generieren. In beiden Fällen wird die Expressionsstärke entweder positiv oder negativ beeinflusst, was letztlich einen Einfluss auf die gesamte Funktion der Zelle haben kann.
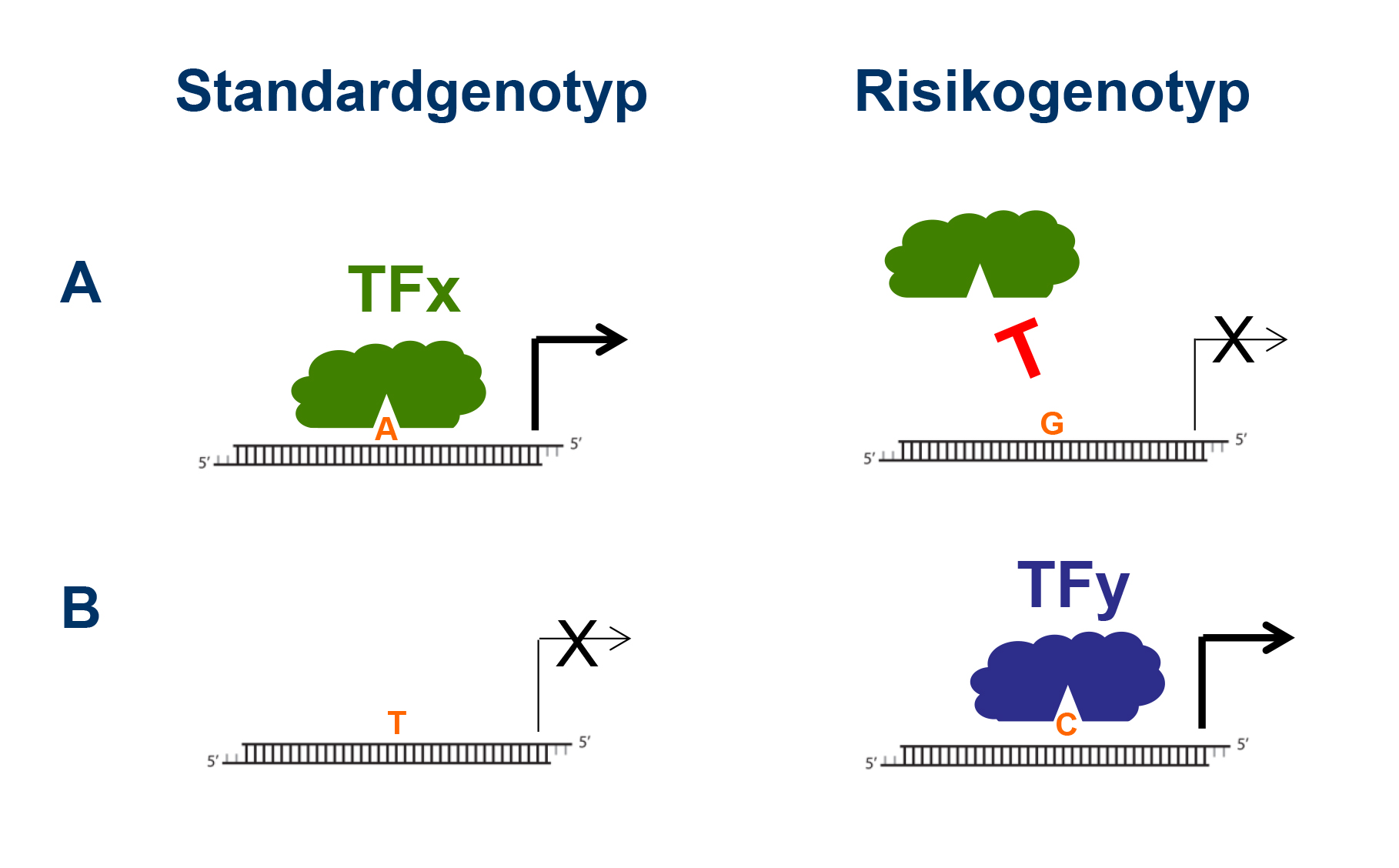
(A) Während im Standardgenotyp ein spezifischer Transkriptionsfaktor (TFx) an eine regulatorische DNA-Sequenz bindet, wird im Falle des Risikogenotyps die Bindung durch einen Basenaustausch (SNP) verhindert. Dadurch kann der Transkriptionsfaktor nicht mehr das Gen aktivieren, es kommt zu einer verringerten Genexpression.
(B) Alternativ kann durch einen SNP auch eine neue Bindungsstelle für einen Transkriptionsfaktor (TFy) entstehen. Dadurch wird die Expression eines in der Nähe liegenden Gens erhöht.
In diesem Teilprojekt führen wir eine proteomweite Analyse von Atherosklerose-assoziierten SNPs (PWAS) durch, um durch SNPs verursachte differentielle Bindungen von Transkriptionsfaktoren aufzudecken und deren Einfluss auf die Zellfunktion zu verstehen. Außerdem wollen wir von ausgewählten SNPs deren Funktion während der Atherogenese studieren. Unser Hauptinteresse gilt dabei zwei SNPs, welche in regulatorischen Bereichen der Gene HDAC9 und ADAMTS-7 liegen. Während HDAC9 ein Enzym im Zellkern darstellt, welches selbst an der Regulation anderer Gene beteiligt ist, handelt es sich bei ADAMTS-7 um ein Protein, das sich in der extrazellulären Matrix befindet, welche eine Struktur aus Proteinen, Zuckerketten und Signalmolekülen darstellt. Für beide SNPs wurde in genomweiten Assoziationsstudien ein signifikanter Zusammenhang mit klinischen Manifestationen einer Atherosklerose (Schlaganfall und Koronare Herzerkrankung) nachgewiesen. Zwischenzeitlich konnten wir und andere zeigen, dass das Abschalten von HDAC9 im Mausmodell zu einer Attenuierung von Atherosklerose führt. In ähnlicher Weise haben erste Untersuchungen mit ADAMTS-7 gezeigt, dass Mäuse, in denen ADAMTS-7 nicht exprimiert wird, eine geringer ausgeprägte Gefäßrestrukturierung nach Gefäßschädigung aufweisen. Unser Augenmerk gilt daher dem Verständnis sowohl von der Regulation dieser beiden Proteine als auch von ihren jeweiligen molekularen Funktionen im Kontext der Atherogenese.
Das Ziel dieses Teilprojektes ist letztlich die Entschlüsselung neuer molekularer Signalwege, um so geeignete Angriffspunkte zur Diagnose und Theraphie von Atherosclerose zu finden.
Keywords: Atherosklerose, atherosclerosis single nucleotide polymorphism, SNP



