TIL-REP
Dynamik des Repertoires Tumor-infiltrierender Lymphozyten in Melanom und Pankreaskarzinom
Die Anwesenheit Tumor-infiltrierender Lymphozyten (TIL) ist in vielen Krebserkrankungen mit einem besseren Überleben assoziiert. Dies deutet darauf hin, dass das Immunsystem Krebs erkennen und bekämpfen kann. In fortgeschrittenem Krebs dominiert jedoch häufig Immunsuppression, wobei beispielsweise TILs außer Gefecht gesetzt werden, indem Tumorzellen hemmende Faktoren ausgeschütten.
Therapeutische Ansätze versuchen, dies rückgängig zu machen, z.B. durch Blockade negativer Signale mit therapeutischen Antikörpern (z.B. Ipilimumab). Auch die in vitro Expansion (Vermehrung) und Re-Infusion von TIL (sog. TIL-Therapie) kann die anti-tumorale Immunantwort (re)aktivieren.
Unter solch optimierten Bedingungen kann das Immunsystem das Tumorwachstum auf beeindruckende Weise hemmen und das Tumorleiden selbst in metastatischen Krebsstadien wirksam reduzieren; dies ist insbesondere im malignen Melanom gut beschrieben. Viele Studien haben gezeigt, dass der Erfolg solcher Therapien auf der Anwesenheit Tumor-reaktiver T-Zellen basiert. Welche T-Zellen genau für diese positiven Effekte verantwortlich sind, ist jedoch noch nicht vollständig bekannt.
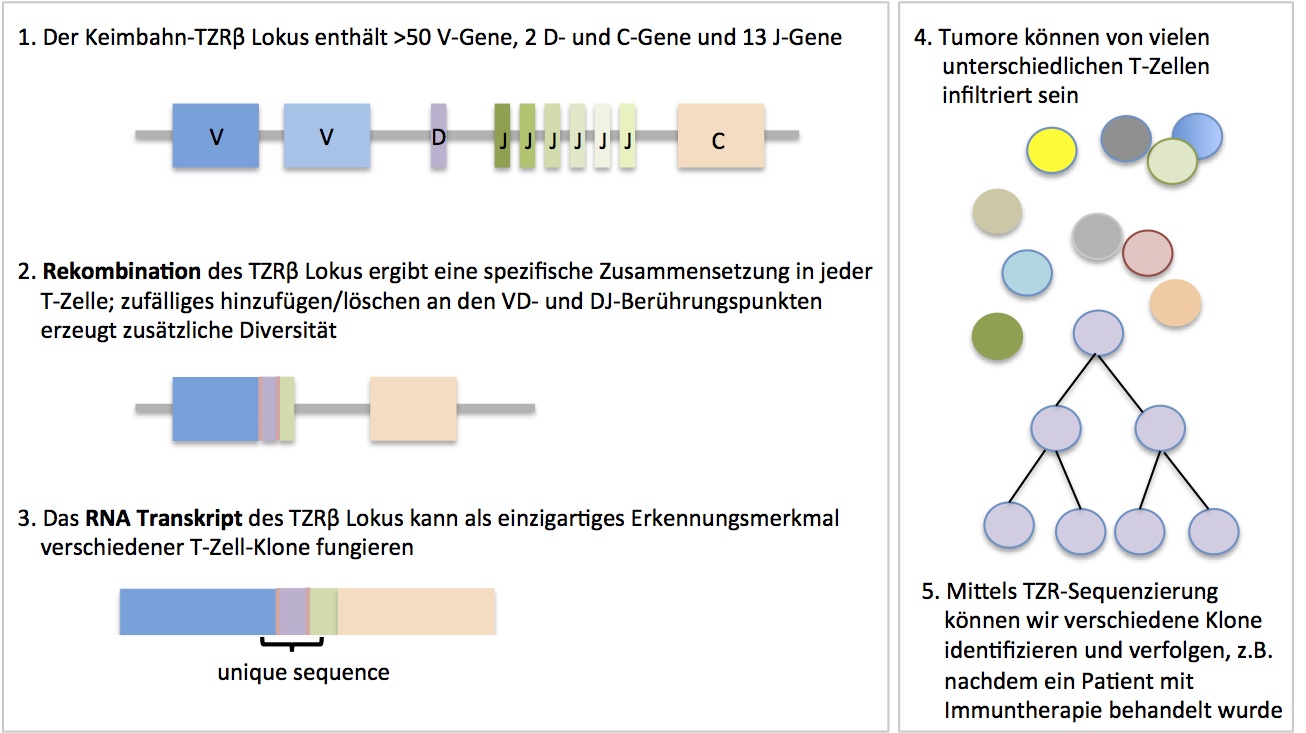
1-3. Jede T-Zelle wird mit einem einzigartigen Rezeptor ausgestattet. 4. Wird die T-Zelle, z.B. durch Interaktion mit dem Tumor, aktiviert, beginnt sie sich zu teilen. Dadurch entsteht ein sog. T-Zell-"Klon", dessen Zellen alle den gleichen Rezeptor tragen. 5. Wieviele Zellen den gleichen Rezeptor tragen, also die Klon-"Größe", kann mithilfe von T-Zell-Rezeptor-Sequenzierung gemessen werden.
* Der T-Zell Rezeptor besteht aus alpha und beta Kette/Untereinheit, die in ähnlichen Prozessen rearrangiert werden; unter 1-3 ist nur die beta-Kette gezeigt.
Das TIL-REP Konsortium wird die Zusammensetzung und dynamische Veränderung des TIL Repertoires sowie deren klinische Bedeutung erforschen. Wir verfolgen dabei drei komplementäre Strategien:
- Analyse des TIL Repertoires in humanen Tumorbiopsien des malignen Melanoms und des duktalen Pankreas-Adenokarzinoms durch Phänotypisierung (Messung characteristischer Oberflächen- und Aktivierungsmarker) und T-Zell-Rezeptor (TZR) Sequenzierung (s. Abb. 1)
- Untersuchung klonaler Veränderungen/Dynamik der TIL-Antwort in präklinischen Tumormodellen
- Entwicklung Daten-basierter mathematischer Modelle, welche die Entstehung des TIL-Repertoires beschreiben, quantifizieren und seine Veränderung durch immuntherapeutische Ansätze vorhersagen.
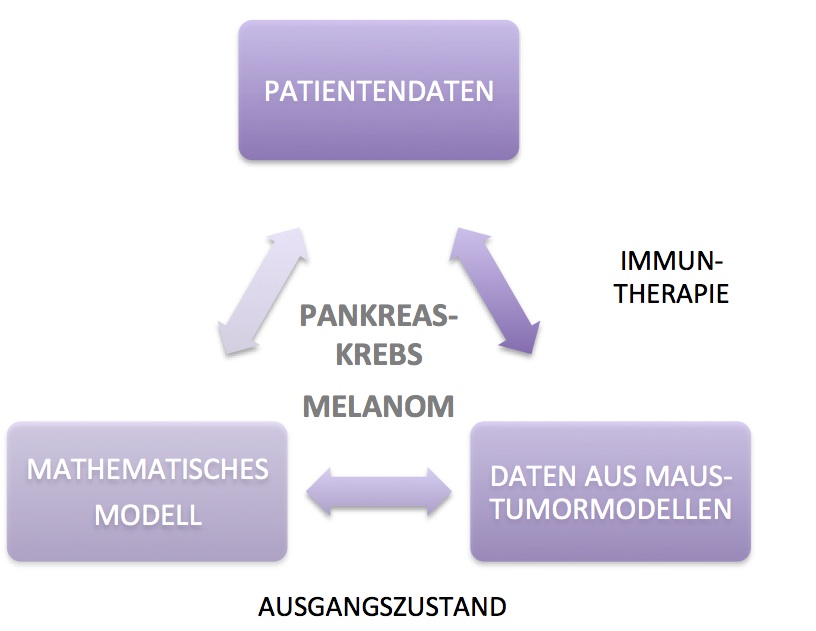

Unser systemmedizinischer Ansatz (s. Abb 2) unter Berücksichtigung von Modellorganismen, mathematischen Modellen und Patientenproben soll helfen, Tumor-Immun-Interaktionen besser zu verstehen, Biomarker für den Erfolg von Immuntherapien zu entwickeln und in Zukunft die Therapie von Krebspatienten zu verbessern.
Um diese Ziele zu erreichen, arbeiten wir in einem interdisziplinären Team, welches unsere Fragestellung von theoretischer, (zell)biologischer und klinischer Seite beleuchtet (s. Abb 3).

Teilprojekte in TIL-REP:
TP 1 TIL Dynamik in einem Mausmodell für malignes Melanom
TP 2 Entwicklung eines mathematischen Modells der anti-Tumor T-Zell Antwort
TP 3 Charakterisierung des TIL Repertoires in Melanom und Pankreaskarzinom
TP 4 Zusammenhang von TIL Repertoire und Behandlungserfolg in Melanompatienten
TP 5 TIL Dynamik im Pankreaskarzinom
Keywords: Tumor-infiltrierende Lymphozyten, Immuntherapie, T-Zell Rezeptor Repertoire, next-generation Sequenzierung, Pankreaskrebs, Melanom, Imfpung, immunstimulatorische Antikörper



