TP 4
Herstellung und Validierung von therapeutisch relevanten neuartigen TRAIL- Fusionsproteinen
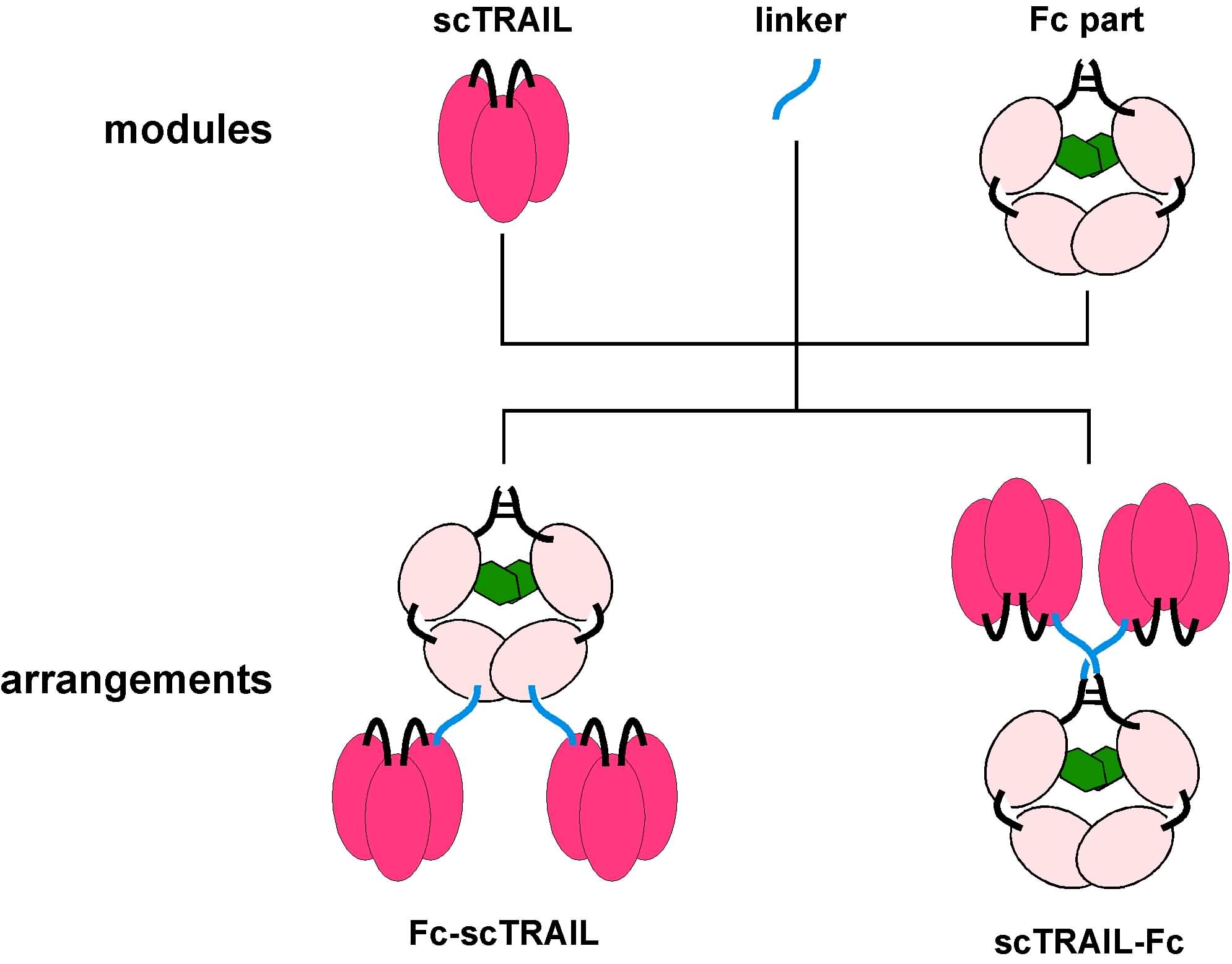
Bei der Entwicklung neuer, hochwirksamer Medikamente für die Therapie von Tumorerkrankungen einschließlich des Melanoms gelten immuntherapeutische Ansätze auf der Basis pro-apoptotischer (d.h. Zelltod-auslösender) und immunstimulierender Zytokine der Tumornekrosefaktor (TNF) Familie als sehr aussichtsreich, vor allem in Kombination mit Chemotherapie. Bei den proapoptotischen Zytokinen wird dem TRAIL Molekül aufgrund seiner potentiell tumorselektiven Wirkung eine besondere Bedeutung zugeschrieben. Vorausgehende Arbeiten über Grundlagen der Bildung signalfähiger Ligand-Rezeptorkomplexe haben Lösungswege aufgezeigt, die hier genutzt werden, um hochaktive, stabile und tumorselektiv wirksame rekombinante TRAIL Moleküle herzustellen. Die Grundlage ist die Konversion von einem nicht kovalent zusammengelagerten Homotrimer in ein einzelsträngiges, durch kurze Peptidlinker kovalent verknüpftes Molekül, sc (single chain) TRAIL. Auf diesem Basismodul lassen sich durch weitere gentechnische Verknüpfungen bi- und multifunktionelle Moleküle herstellen, z.B. um die spez. Aktivität zu steigern oder um Tumorspezifität zu gewährleisten. Beim Design dieser neuen TRAIL Moleküle werden neben der Aktivität auch pharmakolkinetische Eigenschaften berücksichtigt, um die beste therapeutische Wirkung zu erzielen und Nebenwirkungen zu minimieren. Im Projekt werden verschiedene Fusionsproteine bestehend aus 2 scTRAIL, also hexavalentes scTRAIL, u.a. unter Verwendung des Antikörper Fc Teils als Dimerisierungsmodul in unterschiedlichen Formaten entwickelt (Fc-scTRAIL, scTRAIL-Fc) und den Partnern zur Verfügung gestellt. In dieser Konfiguration wird die Eigenschaft der Fc Komponente, eine lange Plasmahalbwertszeit zu verursachen, ausgenutzt. Prototypen werden durch weitere gentechnische Änderungen bzgl. der Stabilität, Produzierbarkeit und der funktionellen Eigenschaften optimiert.
Diese Arbeiten umfassen eine umfangreiche biochemische Charakterisierung, in vitro Apoptose-Induktion in Kombinationsbehandlung sowie in vivo Versuche zur Pharmakokinetik. Gemeinsam mit den Projektpartnern wird die Gewebepenetration des Wirkstoffs in in vitro 3D Melanomkulturen und in ex vivo kultivierten Biopsien immunhistochemisch analysiert. Ziel des Teilprojektes ist es, einen der hier entwickelten hexavalenten TRAIL-Rezeptor Agonisten nach erfolgreicher in vitro und in vivo Testung als präklinischen Entwicklungskandidaten zusammen mit einem Pharma- bzw. Biotechpartner zu entwickeln bzw. auszulizensieren.



