TP4 - NephrESA
Submodell der Dynamik der Thrombozytenaktivierung bei CKD-Patienten
Da CKD-Patient:innen häufig unter Blutarmut (Anämie) leiden, erhalten sie Arzneimittel aus der Gruppe der Erythropoese-Stimulatoren (ESA). Diese regen eine Bildung roter Blutkörperchen (Erythrozyten) an. Zu den Nebenwirkungen der ESA gehören unter anderem ein erhöhtes Thromboserisiko. Um die medikamentöse Therapie zu optimieren und künftig besser individuell auf die Betroffenen zuzuschneiden, untersuchen die Wissenschaftler:innen am Leibniz-Institut für Analytische Wissenschaften – ISAS – e.V. die Thrombosegefahr.
Bei einer Thrombose gerinnt das Blut und verstopft als Blutgerinnsel (Thrombus) ein Gefäß. Verantwortlich für diesen Vorgang sind bestimmte Proteine an der Zelloberfläche der Blutplättchen (Thrombozyten), die ihre Aktivierung steuern und so verklumpen. Die Folgen können als Lungenembolie, Schlaganfall oder Herzinfarkt lebensbedrohlich sein.
Je nach Erkrankungsgrad haben CKD-Patient:innen, die zumeist unter Blutarmut (Anämie) leiden und daher mit Epo behandelt werden, ein zwei bis dreimal höheres Risiko für eine Thrombose als andere Menschen. Der Grund dafür ist, dass die Aktivierung und die Zusammenlagerung (Aggregation) der Thrombozyten bei ihnen durch die Therapie mit ESA erhöht sind. Die Behandlung mit ESA, die den Patient:innen bei ihrer Nierenerkrankung helfen soll, birgt somit eine Thrombosegefahr.
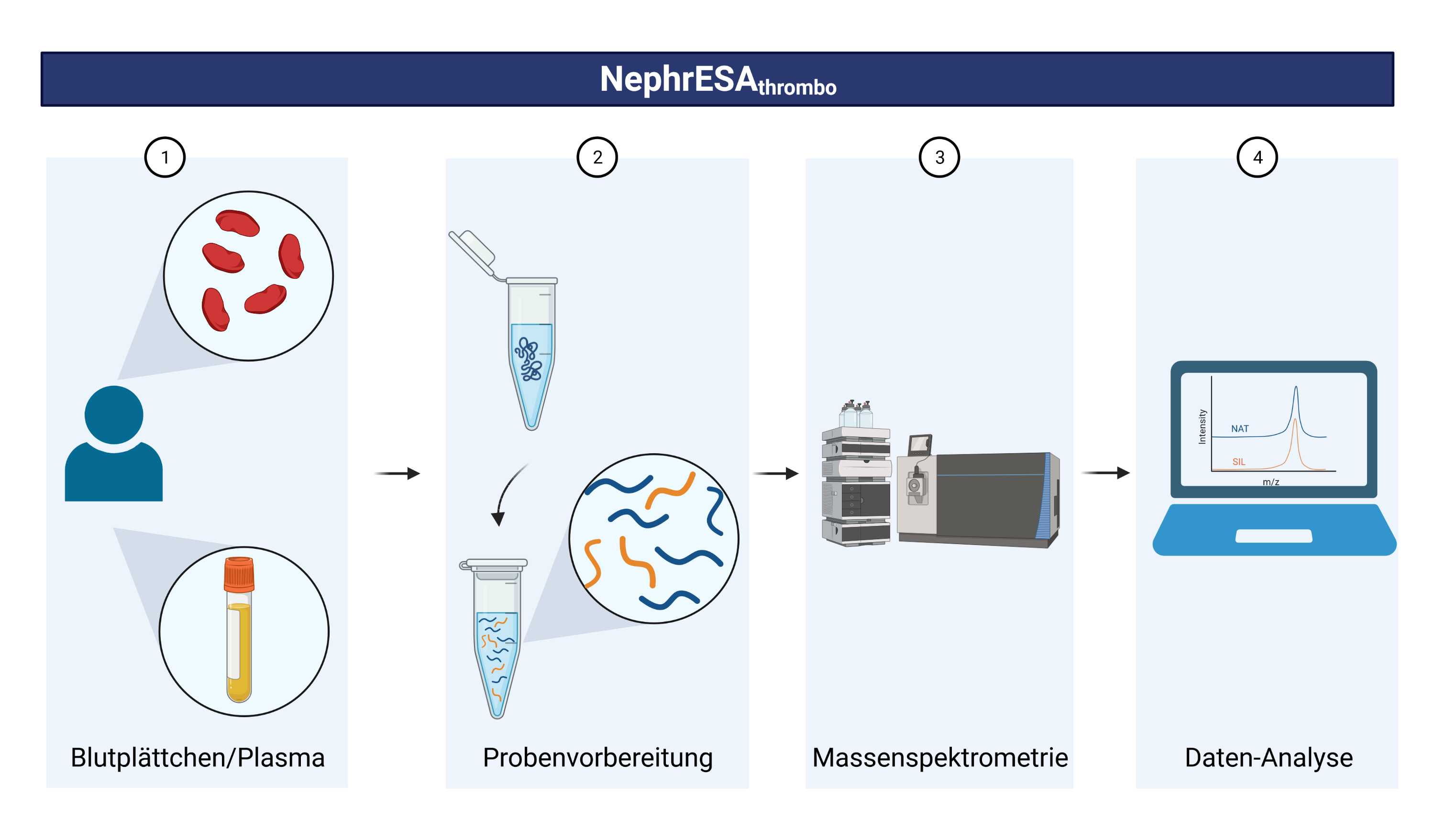
Im Teilprojekt 4 (TP4) am ISAS geht es um den bislang unerforschten molekularen Mechanismus, der dafür sorgt, dass die Thrombozyten bei CKD-Patient:innen aus dem Gleichgewicht geraten. Die Forscher:innen untersuchen mittels Massenspektrometrie Blutplasma und Thrombozyten von CKD-Patient:innen, um Marker für die frühzeitige Aktivierung der Blutgerinnung zu identifizieren. Ziel ist es, damit Patient:innen künftig eine personalisierte Anämiebehandlung mit der niedrigsten Thrombosegefahr zu ermöglichen.
Die Hauptziele sind:
1. Entwicklung von Testsystemen (Assays) für Blutplasma-Risikofaktoren für thrombovaskuläre (Blutplättchen und Gefäße betreffende) Ereignisse.
2. Entwicklung von Assays für den Aktivierungsstatus von Thrombozyten bei CDK-Patient:innen.
3. Analyse von Veränderungen in der Dynamik der Thrombozyten-Aktivierung bei CKD-Patient:innen.
4. Entwicklung eines Computermodells (NephrESAthrombo-Submodell) des thrombovaskulären Risikos für CKD-Patient:innen.