TP4 - SysMedSUDs
In silico Vorhersage dynamischer Veränderungen in multiskaligen neurochemischen Konnektomen in SUDs
Trotz verschiedener molekularer Wirkmechanismen wirken Drogen auf unterschiedliche, jedoch teilweise überlappende neuronale Netzwerke. Wir haben gezeigt, dass das Verlangen nach psychoaktiven Substanzen mit der Aktivierung spezifischer hirnweiter Netzwerke zusammenhängt, die zugrundeliegende Neurobiologie jedoch weiterhin schwer fassbar ist. In diesem Teilprojekt wenden wir mathematische Modelle und Simulationen an, um zu untersuchen, wie eine akute und chronische Exposition von verschiedenen Drogen (Alkohol, Nikotin, THC, Heroin und Kokain) die zelluläre Aktivität verändert, insbesondere im Hinblick auf kurzfristige und anpassende Veränderungen in Neurotransmitterkonzentrationen. Dabei verwendet unser mathematisches Modell, das aus einem Satz gekoppelter nichtlinearer Verzögerungsdifferentialgleichungen besteht, zwei massive Datenbanken. Durch das Screening von 338.982 Veröffentlichungen haben wir systematisch Daten von 147.138 Ratten gesammelt, die in zwei Open-Access-Datenbanken integriert wurden: www.chemnetdb.org und www.syphad.org. ChemNetDB wird als topologische Grundlage unseres Modells dienen, da es einen einzigartigen, umfassenden Rahmen für die effektive Untersuchung des normalen und erkrankten Gehirns bietet. Die Syphad-Datenbank enthält detaillierte neurochemische Fingerabdrücke von Psychopharmaka und wird als Grundlage für Algorithmen für maschinelles Lernen zur optimalen Identifizierung von Modellparametern verwendet. Für unterschiedliche Muster der Drogeneinnahme und unterschiedliche Konzentrationen prognostiziert unser patentiertes in silico-Verfahren für jede Gehirnregion die zeitlichen Verläufe der Konzentrationen verschiedener Neurotransmitter, insbesondere Aminosäuren, Monoamine und Neuropeptide. Diese neurochemische Entschlüsselung von drogeninduzierten Veränderungen im Gehirn von Ratten verbessert unser Verständnis der unterschiedlichen, überlappenden und zeitabhängigen Wirkmechanismen von Drogenmissbrauch auf Systemebene und ebnet den Weg für die Entwicklung optimaler Behandlungsstrategien für die Rückfallprävention.
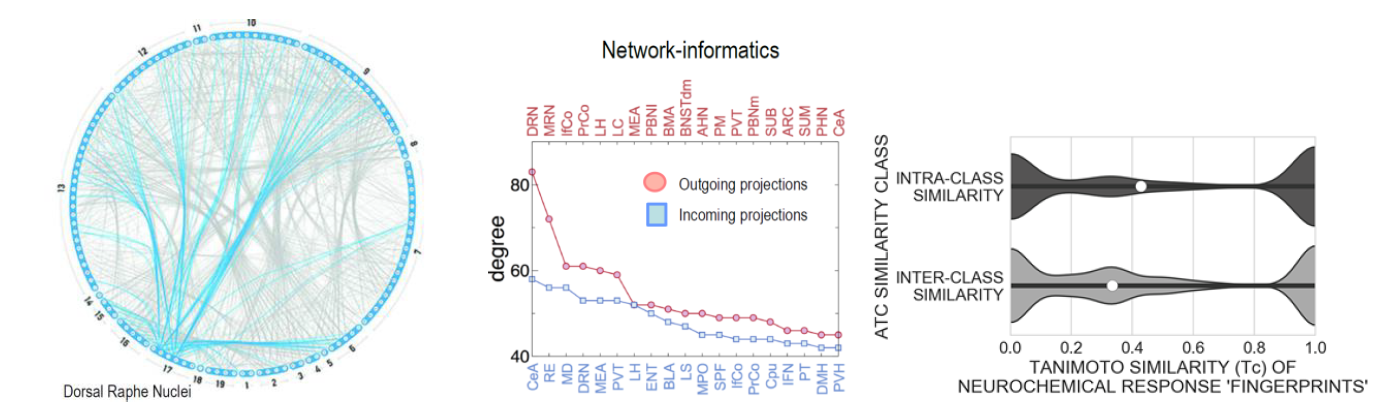

Das neurochemische (Neurotransmitter-basierte) Konnektom des Rattenhirns und seiner Netzwerkeigenschaften und neurochemische Fingerabdrücke von Psychopharmaka (ausführlich beschrieben in unseren jüngsten Studien von Noori et al., 2017; 2018). Linker Teil: Schematische Darstellung des neurochemischen Konnektoms durch ein Konnektogramm mit 125 Knoten (Hirnregionen), aufgeteilt in 19 großräumige Hirnregionen. Dargestellt sind nur serotoninerge Verbindungen, die hauptsächlich von Knoten-Raphe-Kernen stammen, der Quelle serotoninerger Fasern. Der mittlere Teil zeigt Diagrammeigenschaften mit In- und Out-Grad-Rangfolge. Zum Beispiel hat der dorsale Raphekern (DRN) mehr als 80 ausgehende Projektionen und die zentrale Amygdala (CeA) hat die meisten eingehenden Projektionen im Rattenhirn. Der rechte Teil zeigt den Intra- und Inter-ATC-Code (ATC bezieht sich auf das Anatomical Therapeutic Chemical Classification System), Ähnlichkeiten der neurochemischen Antwortmuster über Gehirnregionen (mittlere Ähnlichkeiten werden durch den weißen Marker identifiziert). Neurochemische Fingerabdrücke werden auch für alle 5 Drogen nach langfristiger Selbstverabreichung im Wiedereinsetzungsparadigma berechnet, sodass wir quantitative Schlussfolgerungen über ihre Ähnlichkeiten ziehen können.



